عزيزي القارئ اذا اردت ان تعرف ان العدد الذري يساوي رقما ..؟ لذلك سنجيب عليك على هذا السؤال الذي انتشر بشكل كبير في محركات السيرش الإلكترونية ، بالنظر لـ وجود مادة العلوم في مناهجها الأكاديمية في أسئلة طلاب المملكة العربية السعودية.
حدث ذلك عقب أن وضحت الحكومة السعودية نظام التعليم عن بعد أو منصة مدرستي التي تقدم حاليًا كل دروس التعليم بشكل إلكتروني حديث دون الحاجة لـ الذهاب لـ المدرسة ، فضلًا عن إثارة هذا السؤال وفضول الكثيرين ، وليس الطلاب فقط.
لـ جوار توضيح أهمية رقم الذري والفرق بينه وبين رقم الكتلي ، سنشرح مفهوم العدد الذري وكيفية إيجاده وحسابه ، وكذلك شرح الإجابة النموذجية على هذا السؤال عبر موقعنا الإلكتروني ، ستجد كل هذه البيانات في السطور الموجودة أسفل هذا المقال ، تابعنا.
العدد الذري يساوي رقم هاتفًا واحدًا
المحتويات
بينما انتشر هذا السؤال مؤخرًا عبر محركات السيرش الإلكترونية للعثور على الإجابة ، سواء لحل أسئلة كتاب العلوم للطالبات والطالبات في المملكة أو للعثور على إجابة لهذا السؤال ، فإن إجابة سؤالك جاءت على النحو التالي:
- الجواب هو هذا: العدد الذري للدورة يساوي مجموعة البروتونات وكذلك مجموعة الإلكترونات.
العدد الذري والعدد الكتلي للعناصر
نظرًا لأن العدد الذري للعناصر هو مجموعة البروتونات في نواة ذرة واحدة ، فإنه يحدد خصائص وخصائص العناصر المختلفة ، نعبر عن مجموعة البروتونات P في الذرة بالرقم الذري Z ، وهو الرمز Z.
- العدد الكتلي هو مجموع مجموعة P نيوترونات ، الذي نسميه N ، وعدد البروتونات في النواة ، بالإضافة لـ الكتلة الدائرية للعناصر التي تحمل الرمز A.
قانون العدد الذري
نجد العدد الذري في أي عنصر من عناصر الجدول الدوري عبر رقم الموجود أسفل رمز العنصر نفسه ، لأنه يمثل مجموعة البروتونات ، على سبيل المثال عنصر الهيدروجين H ، نجد أنه يحتوي على بروتون واحد فقط.
- إذن ، العدد الذري للهيدروجين هو 1.
- مثال انتهاء هو الكربون الذي يحتوي على ستة بروتونات في نواته ، لذلك نجد أن عنصر الكربون له رقم هاتف ذري 6 ، وهكذا.
- من الجدير بالذكر أن العدد الذري لكل عنصر في الجدول الدوري هو رقم هاتف ثابت بكمية لا تتغير أبدًا ، مما يشير لـ الكمية الثابتة من البروتونات داخل نواة كل عنصر في الجدول الدوري.
طريقة حساب العدد الكتلي
نحسب الكتلة الذرية أو مجموعة الكتلة لأي عنصر في الجدول الدوري بمعادلة بسيطة على النحو التالي:
- الكتلة الذرية A = مجموعة النيوترونات N + P مجموعة البروتونات.
- على سبيل المثال: تحتوي ذرة الهليوم على بروتونين في نواتها ، بالإضافة لـ نيوترونين ، فإن مجموعة كتلة ذرة الهيليوم هو He = مجموعة البروتونات + مجموعة النيوترونات 2 = وبالتالي فإن الكتلة الذرية لعنصر الهيليوم تساوي 4.
أهمية العدد الذري
كما ذكرنا سابقًا ، بالرغم من أن العدد الذري مهم جدًا في تحديد خصائص وخصائص العناصر في الجدول الدوري ، إلا أنه مهم جدًا أيضًا في تحديد عنصر الذرة من خلاله.
- ومع ذلك ، فإن الجدول الدوري الحديث الذي تنتسب إليه كل المؤسسات والمنظمات في العالم ، إن لم يكن كلها ، يعتمد كليًا على العدد الذري ، لذلك فهو قائم ومرتفع من اليسار لـ اليمين.
العدد الذري للماء
كثير من الناس يريدون حضور العدد الذري للماء ، لذلك فإن الأمر مبني على قانون إيجاد العدد الذري لكل عنصر ، وهنا نشرح طريقة حساب العدد الذري للماء h2o على النحو التالي:
- ينقسم مركب الماء لـ مكونين:
- عنصر الأكسجين O2.
- عنصر الهيدروجين H
- نظرًا لأننا نحتاج لـ حساب كل من ذرات O2 و Hydrogen H بشكل منفصل:
- يحتوي عنصر الأكسجين على 16 بروتونًا في نواته O2 ، مما يعني أن العدد الذري هو 16.
- يحتوي عنصر الهيدروجين H على بروتون واحد في نواته ، مما يشير لـ أن العدد الذري هو 1.
- إذا استنتجنا مما سبق أن العدد الذري لمركب الماء H2O هو 16 + (2 × 1) ، فإن العدد الذري للماء هو 18 لأن عنصر الهيدروجين يحتوي على ذرتين في مركب الماء.
الجدول الدوري مع العدد الذري والكتلي
قام العالم الكيميائي الروسي ديمتري مندليف بترتيب عناصر الجدول الدوري بناءً على سلوك وخصائص الصفات الموجودة في العناصر والمشار إليها بوضوح في العدد الذري لكل عنصر ، بالإضافة لـ العدد الكتلي لكل عنصر من العناصر في الجدول ، لكن العالم لم يرتبهم بالأرقام الذرية. والكتلة ، ولكن فقط بسلوكه ، وتوفي مندليف عام 1907.
- وصل الكيميائي هنري موسلي في عام 1913 بعد حوالي 6 سنوات من وفاة العالم منديليف ، ووضع عناصر الجدول الدوري مرتبة حسب الأعداد الذرية ، فنانة بعدد البروتونات الموجودة في كل عنصر من عناصر الجدول.
- قام العالم هنري موزلي بتعريض العناصر مباشرة لـ حزمة من الإلكترونات عبر جهاز يسمى مدفع الإلكترون اليوم ، حيث تم قياس مجموعة البروتونات في الذرات بشكل واضح وسهل.
- بينما يظهر لك شكل الجدول الدوري الحديث كالتالي:
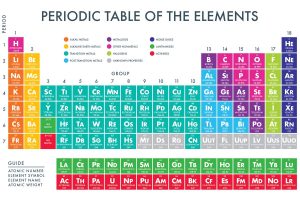
عزيزي القارئ نأتي لـ خاتمة هذه المقالة التي تركز على إذاعة إجابة نموذجية لسؤالك: العدد الذري يساوي مجموعة ..؟ كما ناقشنا في مقالتنا ، شرح وتعريف مفهوم الإجابة النموذجية والعدد الذري والعدد الكتلي بشكل منفصل عن المناهج والمناهج الدراسية لطلاب المملكة العربية السعودية.